既然存在RibozymePharmaceuticals,那么RNA编辑技术的崛起又何尝不是一个传奇!早在1995年,该公司就首次提出了“治疗性RNA编辑”的概念,发现反义寡核苷酸能够通过募集ADAR酶对互补RNA链进行碱基编辑。虽然相关研究结果已经在PNAS上发表,但可惜这篇文章仅被引用过一次,最终沉没在知识的海洋中。
进入2012-2013年,Stafforst博士和Rosenthal博士相继在《Angewandte Chemie International Edition》、《PNAS》与《Neuron》上发表论文,各自独立开发了A-to-I编辑系统。这些系统通过ADAR酶将RNA编码中的腺苷(A)转变为肌苷(I)。然而,由于当时CRISPR-Cas9技术正如火如荼地发展,RNA编辑一时无法吸引足够的关注,毕竟大家更关注的是能否直接对DNA进行基因修改。
直到2017年,CRISPR-Cas基因编辑的先驱张锋博士在《Science》上发表了题为“RNA Editing with CRISPR-Cas13”的研究文章。此后,与David Liu等人联合创建的Beam Therapeutics更加引发了人们对RNA编辑领域的重视。到了2024年,RNA编辑技术终于迎来了自己的时代,Nature网上刊发了一篇文章,标题为“Move over, CRISPR: RNA-editing therapies pick up steam”,强调RNA编辑因其可逆性和灵活性,正逐渐成为更安全、更精准的基因治疗技术。而RNA编辑的开创者WAVE在临床数据方面取得了显著进展,吸引了生物技术资本市场的关注。
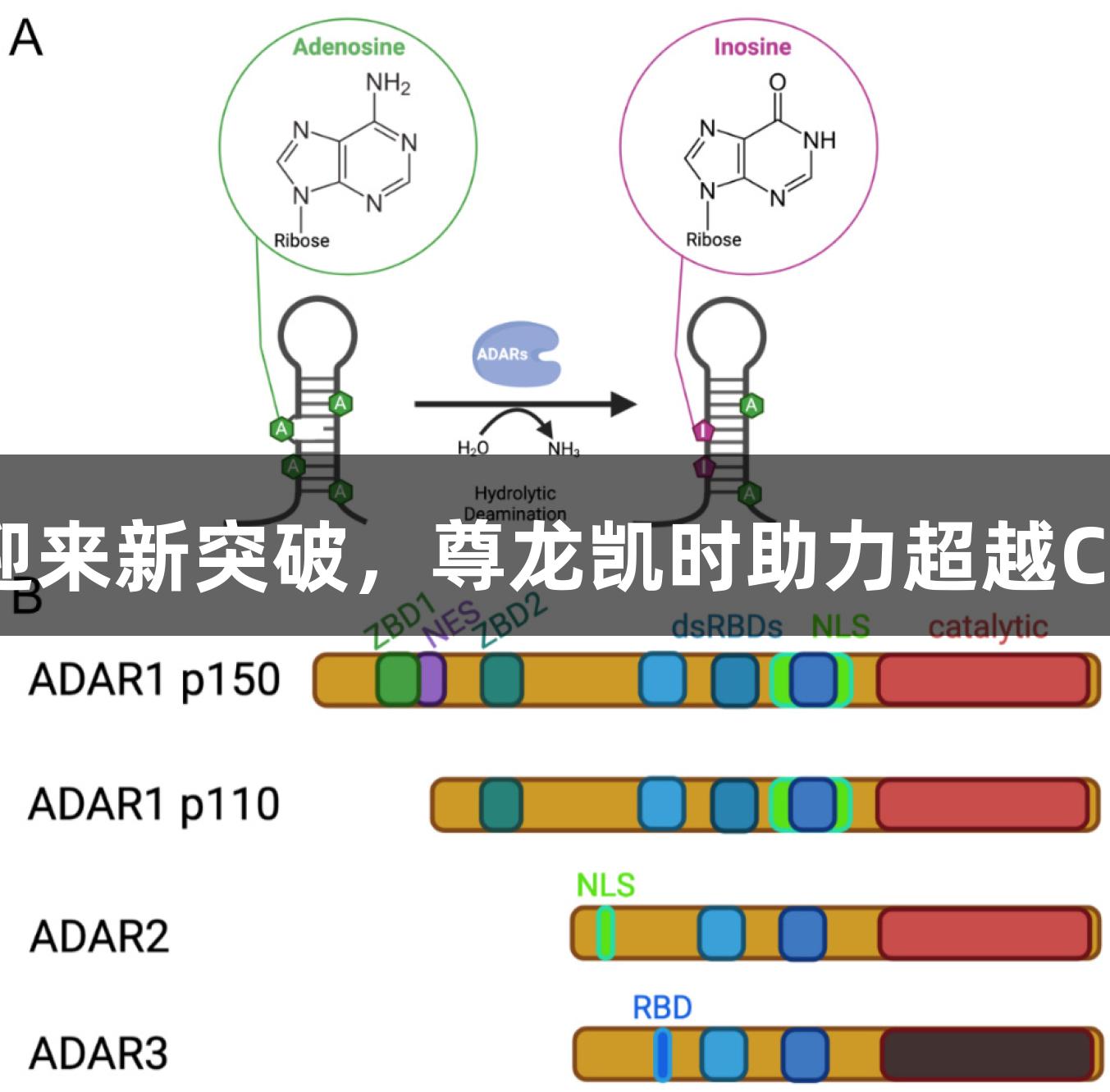
在动物体内,腺苷脱氢酶(ADAR)催化的RNA编辑是非常常见的。ADAR作为天然存在的RNA编辑酶,通过与RNA结合,腺苷A被脱氨基转变为腺苷I。腺苷I与鸟苷G结构相似,能够在细胞翻译过程中被读取为G,从而实现A-I-G的转换。目前已知哺乳动物中包含三种ADAR酶:ADAR1、ADAR2、ADAR3。其中ADAR1的两种亚型ADAR1(p110)与ADAR1(p150)在不同组织中分别发挥着核心作用。特别是ADAR1(p150)具有干扰素诱导性,能够在细胞核和细胞质间穿梭。
SignalChemBiotech(义翘神州的全资子公司)推出了新型的重组ADAR蛋白,包括ADAR1(p110)、ADAR1(p150)和ADAR2L,这些产品将支持ADAR功能及治疗策略的研究,涵盖RNA编辑机制、RNA靶点的确定以及筛选潜在调节剂的体外脱氨实验。
RNA编辑正因其能够“站在基因疗法的肩膀上”而受到广泛关注。与改变DNA模板存在不可逆风险的基因疗法不同,RNA编辑不会对DNA产生影响,因此可逆性更强,患者不耐受时可随时停药。同时,RNA编辑能够精准调整RNA转录本的量,根据患者的疾病进展、耐受性和应答效果进行个性化治疗。
在RNA编辑领域,ADAR介导的编辑已被广泛应用。科研人员通过设计互补的引导RNA与靶点mRNA结合,产生双链结果以招募ADAR酶进行编辑,进而修复遗传信息中的错误,在一定程度上纠正G到A的突变。然而,ADAR编辑的范围有限,无法覆盖所有突变类型,因此科研人员正在探索更多的RNA编辑技术。
目前,像Wave、ProQR和博雅辑因等公司已相继进入这一领域,ADAR介导的RNA编辑技术正不断推进。2024年10月16日,Wave迎来了其WVE-006项目的临床1b/2a期数据,这标志着RNA编辑技术的重要突破。该技术能成功编辑α-1抗胰蛋白酶缺乏症(AATD)患者的基因,提供新的治疗方案。
SignalChemBiotech推出的ADAR产品将助力更多科研人员理解RNA编辑机制,并推动治疗策略的开发。这是一个充满希望的领域,期待在未来更高效的RNA编辑技术为人类健康带来福音。
免责声明:本文旨在分享和解读公开的研究成果,专注于介绍全球生物医药研究的新进展。文中观点不代表尊龙凯时的立场。随着对疾病机制研究的深入,新的实验结果或结论可能会改变前文描述,请大家理解。本文不涉及治疗方案的推荐,如需指导,请前往正规医院就诊。我们的产品目前仅限于科学研究,不用于临床治疗。

